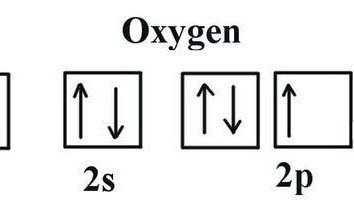
Jak napisać izomery i homologi? Jak być izomery alkanów?
Przed przystąpieniem do badania, jak tworzyć izomery węglowodorów nasyconych ujawnić właściwości tej klasy substancji organicznych.
węglowodory nasycone
wiele klas CxHy stoi w chemii organicznej. Każdy ma wzór ogólny, homologiczne Series, reakcje jakościowe, aplikacji. Do węglowodorów nasyconych alkan klasy Typowy (Sigma) wiązania. Ogólny wzór tych klas substancji organicznych, CnH2n + 2. To wyjaśnia podstawowe właściwości chemiczne: pojemność, spalanie, utlenianie. Dla parafiny nie są typowe łączenie, ponieważ komunikat w cząsteczkach tych węglowodorów pojedyncze.

izomeria
Zjawisko izomerii wyjaśnia różnych substancji organicznych. Zgodnie z izomerii powszechnie rozumiane zjawiska, w którym istnieje kilka związków organicznych mające taką samą liczbę elementów (ilość węgla w cząsteczce), lecz różne ułożenie ich w cząsteczce. Otrzymany materiał jest nazywany izomerów. Mogą być przedstawiciele kilku klas węglowodorów, a więc różnych właściwościach chemicznych. Inne złożone alkany cząsteczek węgla prowadzi do powstania izomerię strukturalną. Jak być izomery alkanów? Istnieje specyficzny algorytm, zgodnie z którym może być reprezentowane przez izomerów strukturalnych o tej klasy substancji organicznych. Istnieje taka możliwość, z czterech atomów węgla, tj cząsteczki butan C4H10.
gatunki izomeryczne
Aby zrozumieć, jak pisać formuły izomerów, ważne jest, aby mieć zrozumienie jego formach. W obecności takich samych atomów w cząsteczce w równych ilościach, które znajdują się w przestrzeni, w innej kolejności odnosi się do izomerii przestrzennej. W przeciwnym razie, to się nazywa stereometrii. W takiej sytuacji, zastosowanie tylko jednej wzorze strukturalnym nie wystarczy, konieczne jest użycie specjalnego występ lub wzorów przestrzennych. Nasyconych węglowodorów poczynając od H3C CH3 (etan), może mieć różne konfiguracje przestrzenne. Jest to spowodowane obrotem w cząsteczce przez wiązania C-C. Jest to prosty σ-wiązanie tworzy konformację (obrotowe) izomery są możliwe.

strukturalnych izomerów parafiny
Porozmawiajmy o tym, jak tworzyć izomery alkanów. Klasa ma izomeru strukturalnego, to jest tworzy inny łańcuch atomów węgla. W przeciwnym przypadku, możliwość zmiany pozycji w łańcuchu atomów węgla w szkielecie węglowym zwany izomerię.
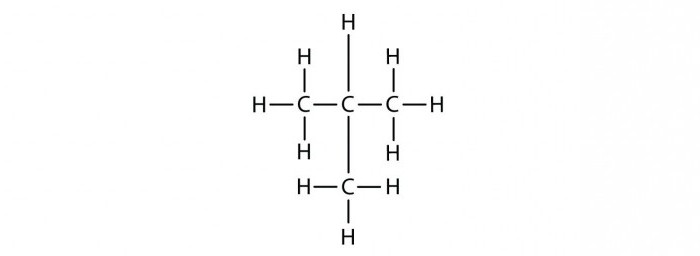
izomery heptanu
Więc, pozostawiając izomery substancji o składzie C7H16? Na początek, można zorganizować wszystkie atomy węgla w jeden długi ciąg, należy dodać do siebie pewną liczbę atomów C Ile? Biorąc pod uwagę fakt, że węgiel jest wartościowość równą cztery, w ekstremalnych do trzech atomów węgla, wodoru i co wewnętrzna – dwa. Otrzymany cząsteczka posiada strukturę liniową, węglowodór o nazwie N – heptan. Litera „N” oznacza prosty szkielet węglowy, w węglowodorze.
Teraz zmienić położenie atomów węgla, „skracanie” w tym przypadku prostego łańcucha węglowego w C7H16. Izomery mogą być tworzone w rozszerzonym lub skróconej formie konstrukcyjnej. Rozważmy teraz drugi przykład. Pierwszy atom C zorganizować rodnik metylowy, w różnych pozycjach.
Aktywny izomer heptan, ma następującą nazwę chemiczną: 2-methylhexane. Teraz „przesuwamy” radykalne atom węgla do następnego. Powstały nasycony węglowodór o nazwie 3-methylhexane.
Jeśli nadal będziemy poruszać radykalną numeracja rozpocznie się po prawej stronie (bliżej górnej oznacza rodnik węglowodorowy), czyli mamy ten izomer, co już mamy. Dlatego, myśląc o tym, jak zrobić formułę izomerów materiału wyjściowego, postara się, aby szkielet nawet „krótsze”.
Pozostałe dwa węgla mogą występować w postaci dwóch wolnych rodników – metyl.
Pierwszy rozmieścić je w różnych atomach węgla wchodzących w skład głównego łańcucha. Nazywamy powstały izomer -2,3 dimetylopentan.
Rodnik teraz zostawić w tym samym miejscu i przenieść do kolejnego drugiego atomu węgla w łańcuchu głównym. Materiał ten jest nazywany 2,4 dimetylopentan.
Teraz życzenia rodniki węglowodorowe o jeden atom węgla. Po pierwsze, drugie, uzyskać 2,2 dimetylopentan. Następnie, trzeci otrzymania dimetylopentan 3.3.
Teraz zostawić w łańcuchu głównym czterech atomów węgla, w pozostałych trzech stosowania jako rodniki metylowe. My rozmieścić je w następujący sposób: dwa z drugiego atomu węgla, jeden – trzeci węgiel. Nazwać izomerem uzyskiwanym: 2,2, 3 trimethylbutane.
W przykładzie heptanu omówiono sposób, aby izomery węglowodorów nasyconych. Na rysunku przykłady izomerów strukturalnych przedstawiono na butena6 jego pochodnych chloru.
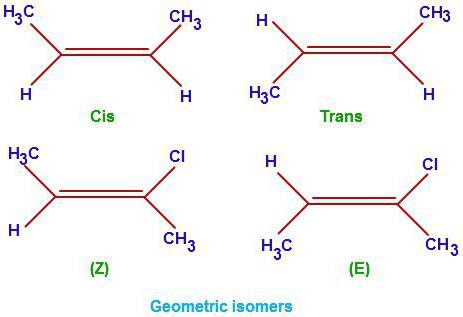
alkeny
Ta klasa związków organicznych ma wzór ogólny CnH2n. Oprócz nasyconych wiązań C-C w tej klasie nie jest wiązaniem podwójnym. Określa on podstawowe właściwości tej serii. Porozmawiajmy o tym, jak opuścić izomery alkenów. Niech ujawni swoje różnice z węglowodorów nasyconych. Dodatkowo do izomerii głównego łańcucha (wzór strukturalny) przedstawiciele tej grupy organicznych węglowodorach, charakteryzuje się również trzech gatunków izomery geometryczne (cis i trans), formy wielokrotnego pozycji wiązania i międzyklasowych izomeru (cykloalkanów).
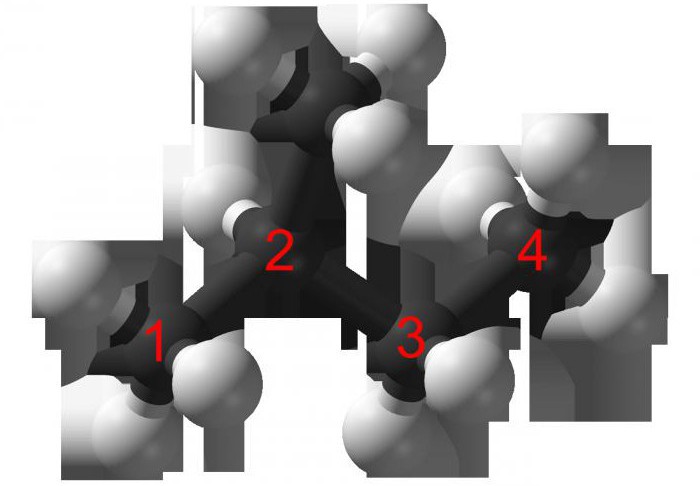
izomery C6H12
Spróbuj dowiedzieć się, jak tworzyć izomery C6H12, biorąc pod uwagę fakt, że substancja wzoru mogą należeć bezpośrednio do dwóch klas związków organicznych: alkenów, cykloalkanów.
Aby rozpocząć, należy zastanowić się, jak być izomery alkenów, jeśli istnieje wiązanie podwójne w cząsteczce. Umieścić prosty łańcuch węglowy, umieścić wiązanie wielokrotne po pierwszym atomem węgla. Staramy się nie tylko do izomery s6n12, ale również wymienić substancję. Materiał – heksan – 1 Liczby oznaczają pozycję w cząsteczce występuje wiązanie podwójne. W swoim ruchu w łańcuchu węglowym, heksen uzyskania -2 heksen – 3
Teraz nam myśleć, jak zrobić izomery tego wzoru, zmieniając liczbę atomów w łańcuchu głównym.
Aby skrócić początkowy węgla szkieletu jeden atom węgla, to jest uważana za rodnik metylowy. Podwójne wiązanie po pierwsze dopuszczenie atomu S. Otrzymaną izomer systematycznej nomenklatury będą miały następujące nazwy: 2-metylopenten – 1. teraz przenieść grupę węglowodorową o łańcuchu głównym, pozostawiając niezmienione położenie wiązania podwójnego. Ten nienasycony węglowodór rozgałęzioną strukturę zwaną 3-metylopenten-1.
Jest to możliwe, bez zmiany położenia łańcucha głównego i jednego izomeru podwójne wiązania: 4-metylopenten-1.
Do składu C6H12 może spróbować przesunąć wiązanie podwójne z pierwszej do drugiej pozycji bez przekształcenia się główny łańcuch. Rodnik ten sposób przesuwać wzdłuż szkielecie węglowym, od drugiej atomowy S. izomer ten nosi nazwę 2-metylopenten-2. Ponadto, jest możliwe umieszczenie rodnik CH3 trzecim atomie węgla, z uzyskaniem w ten sposób 3-metylopenten 2
Po umieszczeniu w pozostałości na czwartym atomem węgla łańcucha tworzą inną nową substancję nienasycony węglowodór szkielet węglowy uzwojenia – 4-metylopenten-2.
Przy dalszej redukcji liczby C w łańcuchu głównym, można otrzymać jeden izomer.
Podwójne wiązanie pozostawia po pierwszym atomem węgla, a dwie rodnik dostarczyć trzeci atomem węgla w łańcuchu głównym, dimetiluten uzyskać 3,3-1.
Teraz umieścić rodniki przy sąsiednich atomach węgla, bez konieczności zmiany położenia podwójnego wiązania uzyskania 2,3-dimetylo-butylo 1. Spróbuj bez zmiany rozmiaru łańcucha głównego, podwójny ruch wiązanie do drugiej pozycji. Rodniki więc można dostarczyć tylko 2 lub 3 atomach węgla, o 2,3 dimetylobut-2.
Inne izomery strukturalne dla danego alkenu nie każda próba się z teorią, będzie prowadzić do rozerwania struktury substancji organicznych, A. M. Butlerova.

izomery przestrzenne C6H12
Teraz dowiedzieć się, jak tworzyć izomery i homologi z punktu widzenia izomerii przestrzennej. Ważne jest, aby zrozumieć, że izomery cis i trans alkeny to tylko możliwe w położeniu wiązania podwójnego, 2 i 3.
Podczas gdy w jednej płaszczyźnie rodniki węglowodorowe powstałe cis – mierzona -2-heksylen i rodniki o układzie w różnych płaszczyznach, formy trans-heksen – 2.
Międzyklasowych izomery C6H12
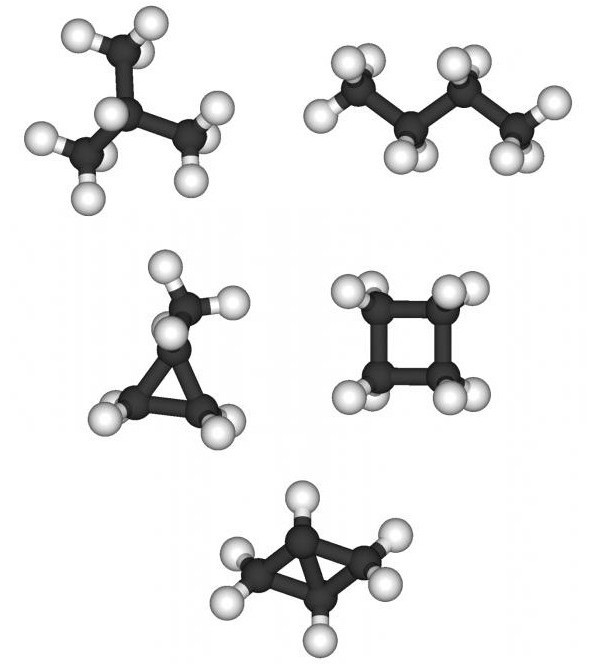
Rozumowanie jak zrobić izomery i homologi nie można zapomnieć o tym rozwiązaniu jako międzyklasowych izomerii. Do nienasyconych węglowodorów szeregu etylenu, mające wzór ogólny CnH2n takie izomery cykloalkanów. Cechą tej grupy węglowodorów obecność struktury cyklicznej (zamknięta pętla) w nasyconym pojedynczym wiązaniem pomiędzy atomami węgla. Można utworzyć formułę cykloheksan, metylocyklopentanu, dimetylocyklobutan, trimetiltsiklopropana.
wniosek
chemia organiczna jest wieloaspektowy, enigmatyczny. Ilość substancji organicznych przekracza setki razy liczbę związków nieorganicznych. Fakt ten można łatwo wytłumaczyć na istnienie takiego unikalnym zjawiskiem w postaci izomerów. Jeżeli homologicznym szeregu rozmieszczone są podobne pod względem struktury i własności substancji, zmieniając pozycję atomów węgla w łańcuchu, to nowe związki nazwane izomerów. Dopiero po teoria struktury chemiczne związków organicznych, zostały sklasyfikowane wszystkich węglowodorów zrozumieć specyfikę każdej klasie. Jednym z postanowień tej teorii, bezpośrednio związane zjawiska izomerii. Wielki rosyjski chemik, był w stanie zrozumieć, wyjaśnić, udowodnić, że położenie atomów węgla zależą od właściwości chemicznych substancji, jej działalności reaktsionanya, praktycznego zastosowania. Jeśli porównamy ilość izomerów utworzona marginalne nienasycone alkany i alkeny, wiodące na pewno alkenów. Powodem jest to, że nie ma podwójne wiązanie w cząsteczce. Że pozwala to klasa materii organicznej, tworząc nie tylko alkeny różnych typów i struktur, ale także mówić o izomerów meklassovoy z cykloalkanów.