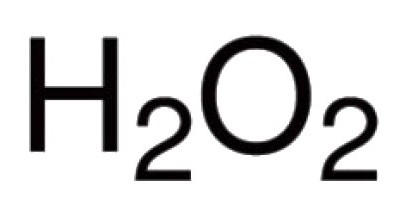W celu określenia wartości możliwych wartościowości tlenu należy rozważyć sytuację elementu w układzie okresowym, główne cechy konstrukcji jej węgla. Takie podejście jest użyteczne w badaniach na pytanie, co wartościowość tlenu w typowy, a co nie jest typowe dla niego. Najczęstszymi związki wykazują normalne wartościowości – II. Ta funkcja pozwala określić liczbę obligacji innym atomem w gotowych formuł binarnych z udziałem tlenu.
Co oznacza wartościowość tlenu?
Na początkowym etapie gromadzenia znajomości właściwości i struktury substancji chemików uważano, że wartościowość – zdolność do wiązania określonej liczby atomów węgla w cząsteczce substancji. Wielu naukowców po odkryciu elementu próbowali zrozumieć, co wartościowość tlenu w. Reakcja otrzymano eksperyment tlen wiąże dwa jednowartościowe atom wodoru, w reakcji chemicznej, oznacza dwuwartościowy. Reprezentacje zróżnicowane wiązanie chemiczne z gromadzeniem wiedzy o strukturze substancji. W teorii wartościowości Lewis i H. W. Kossel ujawnia rodzaj interakcji chemicznej z elektronicznego punktu widzenia konstrukcji. Naukowcy wyjaśniają zdolności pyłku do tworzenia pewnej liczby połączeń dążenie do najbardziej stabilnym stanie energetycznym. W przypadku osiągnięcia najmniejszych cząstek substancji staje się bardziej stabilna. W teorii i struktury Lewisa wiele uwagi poświęca się roli elektronów zewnętrznych uczestniczących w tworzeniu wiązania chemicznego.
Właściwości umieszczania tlenu w układzie okresowym
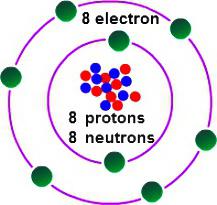
W celu określenia, które mają wartościowość tlenu, konieczne jest, aby rozważyć pewne cechy jego struktury elektronowej. Tlen grupa głowica 16 układu okresowego pierwiastków. Potoczna nazwa członków rodziny – „tlenowców” klasyfikacji przestarzałej należą do VI (A) grupy. W okresowym tlenu w komórce pod №8. Jądro zawiera w swoim składzie 8 i taką samą liczbę pozytywnych obojętnych cząstek elementarnych. W przestrzeni atomu istnieją dwa poziomy energii , które występują, gdy elektrony 8, z których 6 – zewnętrzny.

Co istnieje związek pomiędzy składem atomu i wartościowości?
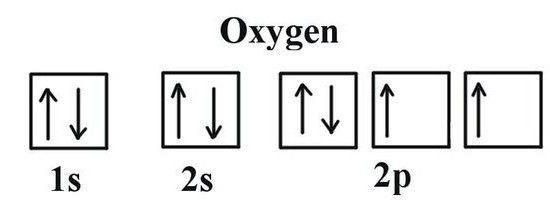
W ostatnim etapie atomu tlenu zawiera dwa niesparowane elektrony. Element fluor jest niższa wartość elektroujemności (zdolność do przyciągania elektronów wiążących para). W tworzeniu związków z innymi pierwiastkami tlenu przyciąga powstały w cząsteczce całkowitej gęstości elektronowej (z wyjątkiem fluoru elektronów). Osiągnięciu stanu ustalonego w zewnętrznej powłoce ewentualnie z dodatkiem dwóch ładunków ujemnych. Oznacza to, że tlen jest wymagane 2 elektrony. Możliwe następujące opcje: przyjęcia jednego elektronu wartościowości (II), z dala od innych atom 2 elektrony (wartościowość II) nie przyjmować elektrony od innych atomów (0 walencyjne). Typowe zachowanie tlenu charakteryzuje drugi przypadek. W ten sposób można użyć, aby dowiedzieć się, co wartościowość tlenu w najbardziej typowy w swoich wspólnych związków. Są to większość tlenków metali i niemetali.
W jaki sposób wartościowość w związkach?
Tlen jest w stanie współdziałać bezpośrednio z wielu pierwiastków chemicznych. Wiadomo jego związków z praktycznie wszystkimi przedstawicielami okresowego (z wyłączeniem gazów obojętnych, argon, hel, neon). Reakcję z halogenów i metali szlachetnych, tlen nie może łączyć się bezpośrednio, a tlenki Au 2O 3, F, Cl 2 O 2 O 7 i istnieją inne (pośredni otrzymany). Dla związków binarnymi powstawania tlenu, który bierze udział, charakteryzuje się wiązaniem kowalencyjnym i polaryzacji. Wartościowość w takich cząsteczek zależy od liczby ewentualnych par elektronów, które są przyciągane do jądra różnymi atomami. W ogromnej większości związków atomami tlenu, są zaangażowane w tworzenie dwóch wiązań kowalencyjnych. Na przykład, tlenki CO 2, P 2O 5, SO2, SO3, K2O, B 2O 3, Mo 2O 5 i innych cząsteczek. W hydroniowych kation H 3 O + tlenu wykazuje nietypowy dla niego wartościowości III. Obecność nadtlenowe spowodowało -OO- niezwykły charakter nadtlenku wodoru H 2 O 2. Związek ten wykazuje charakterystyczne tlenu go wartościowość II.
Jak określić wartościowości pierwiastków?
Pojęcie wartościowości tlenu daje możliwości struktury Lewisa – element WZÓR CHEMICZNY wokół którego elektrony kropki oznaczają zewnętrzną warstwę. biorą udział w tworzeniu cząsteczek, które są częścią wspólną parami elektronów. Wzór Lewisa pokazuje wysycenia tlenem odpowiadającą liczbie jej niesparowanych elektronów (2). Ten sam wynik uzyskano przy użyciu elektronicznych struktur graficznych. Dwie komórki na poziomie zewnętrznej Lambda niesparowanych elektronów (oznaczone strzałkami we wzorze). Aby uzyskać więcej informacji o tym, co wartościowości tlen, co pozwala na końcowym wzoru na wartości binarne związkiem sąsiednich atomów. Aby to zrobić, należy przeprowadzić proste obliczenia. Jest najpierw pomnożona przez liczbę atomów O normalnemu do wartościowości tlenu. Otrzymaną wartość dzieli się przez indeks jak określono we wzorze symbolem chemicznym w pobliżu innego elementu, w połączeniu z tlenem. W prosty sposób obliczyć węgiel i fosfor w wartościowości ich tlenki.
- Pomnożenie wskaźnika w dolnej prawej części dwutlenku znak O CO 2 w typowym elemencie wartościowości 2 • 2 = 4 i wynik podzielenia określonej przez indeks węgla: 4/1 = 4 dwutlenku węgla CO2 jest w stanie najwyższej wartościowości IV ,
- Indeks dolny prawy chemicznego symbolu tlenu w tlenku fosforowego P 2O 5 pomnożyć typowe wartościowość atomów O, 5 • 2 = 10. Ten numer podzielić przez ten wzór w indeksie w prawym dolnym rogu atomów fosforu: 10/2 = 5. tlenku fosforu jest to w najwyższym wartościowości V.