Katalazy – enzym występujący w organizmach żyjących niemal wszystko. Jego główną funkcją – katalizuje rozkład nadtlenku wodoru do substancji nieszkodliwe dla organizmu. Katalaza ma wielkie znaczenie dla życia komórek, ponieważ chroni je przed zniszczeniem przez reaktywne formy tlenu.
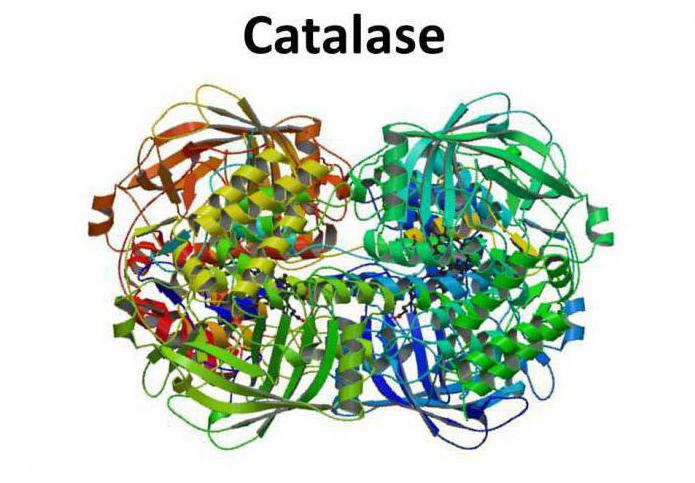
Przegląd
Enzym katalazę dotyczy oksydoreduktazy – szeroką klasę enzymów, które katalizują przeniesienie elektronów z cząsteczką redukującego (donora) na cząsteczkę utleniacza (akceptorem).
Optymalne pH dla katalazy w organizmie człowieka jest około 7, jednak, szybkość reakcji nie zmienia się znacząco przy wartościach indeksu wodoru od 6,8 do 7,5. Optymalne pH dla innych katalazy od 4 do 11, w zależności od rodzaju organizmu. Optymalna temperatura jest różna dla człowieka wynosi około 37 ° C
Katalazy – jeden z najszybszych enzymów. Tylko jedna cząsteczka jest zdolna do przekształcania milionami cząsteczek nadtlenku wodoru do wody i tlenu na sekundę. W warunkach in Enzymology, co oznacza, że duża liczba obrotów charakterystyczne dla enzymu katalazy.
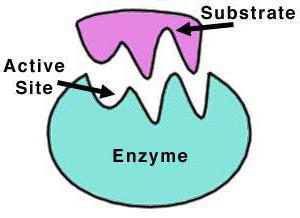
enzym struktura
Katalaza jest tetramerem z czterech łańcuchów polipeptydowych, z których każdy posiada więcej niż 500 aminokwasów. Enzym ten składa się z czterech grup hemu porfiry i przez który reaguje z aktywnych związków tlenu. Utleniona grupa hemu protetyczna jest katalaza.
Historia odkrycia
Katalaza nie była znana naukowcom 1818 roku aż Louis Jacques Thénard chemik odkrył w żywych komórkach nadtlenku wodoru nie sugeruje się, że jego zniszczenia w wyniku działania nieznanego materiału biologicznego.

W 1900 roku niemiecki chemik, Oskar Leo pierwsza wprowadziła „katalazy” termin odnosi się do substancji rozkładających nadtlenek tajemniczą. On był w stanie odpowiedzieć na pytanie, gdzie enzym katalaza zawarte. W wyniku licznych eksperymentów Oskar Leo wykazały, że enzym ten jest charakterystyczny dla prawie wszystkich zwierząt i roślin. W żywych komórkach, a także wielu innych enzymów, katalaza jest zawarty w peroksysomów.
W 1937 roku był pierwszym krystalizować katalazy z wątroby wołowej. 250 kDa – masa cząsteczkowa enzymu oznaczano 1938. W 1981 roku naukowcy otrzymali obrazy struktury trójwymiarowej bydlęcej katalazy.
Kataliza nadtlenku wodoru
Pomimo faktu, że nadtlenek wodoru – produkt z wielu normalnych procesów metabolicznych, nie jest szkodliwe dla organizmu.
 Aby uniknąć zniszczenia komórek i tkanek, nadtlenek wodoru musi być szybko przekształcone w inne, mniej niebezpieczne dla organizmu. Jest to wyzwanie i szpulki enzymu katalazy – rozkłada nadtlenek dwie cząsteczki cząsteczek wody i cząsteczek tlenu.
Aby uniknąć zniszczenia komórek i tkanek, nadtlenek wodoru musi być szybko przekształcone w inne, mniej niebezpieczne dla organizmu. Jest to wyzwanie i szpulki enzymu katalazy – rozkłada nadtlenek dwie cząsteczki cząsteczek wody i cząsteczek tlenu.
Reakcja rozkładu nadtlenku wodoru w żywych tkankach:
2 H2O 2 → 2 H2O + O2
Mechanizm cząsteczkowy enzym rozszczepiania nadtlenku wodoru katalazy nie została jeszcze dokładnie poznana. Zakłada się, że reakcja odbywa się w dwóch etapach – w pierwszym etapie składa się z żelaza katalazy grup prostetycznych związaną z atomem tlenu, nadtlenek, to generuje jedną cząsteczkę wody. W drugim etapie, utleniona hemu oddziaływanie z inną cząsteczką, nadtlenku wodoru, z wytworzeniem innej cząsteczki wody z jedną cząsteczką tlenu.
Poprzez to działanie enzymu katalazy do nadtlenku wodoru, obecność substancji czynnej w próbkach tkanek z łatwością określić. W tym celu wystarczy dodać do badania próbki na małe ilości nadtlenku wodoru, i obserwować reakcję. Obecność enzymu mówi powstawanie pęcherzyków tlenu. Reakcja ta jest dobra, ponieważ nie wymaga żadnych specjalnych narzędzi lub sprzętu – można zauważyć gołym okiem.

Warto zauważyć, że jon wszelkich metali ciężkich może działać jako inhibitor niekonkurencyjne katalazy. Ponadto, wszystkie znane cyjanek zachowuje się jako konkurencyjny inhibitor, katalazy, gdyby w wielu tkankach nadtlenku wodoru. Arseniany działają jako aktywatory.
aplikacja
Działanie enzymu katalaza rozkłada nadtlenek wodoru stosuje się w przemyśle spożywczym, – użycie tego enzymu usuwa się z mleka H 2O 2 do wytwarzania sera. Inna aplikacja – specjalne opakowania do żywności, który chroni produkt przed utlenianiem. Katalaza również stosowane w przemyśle włókienniczym do usuwania nadtlenku wodoru z tkaniny.
Jest on stosowany w higienie soczewek kontaktowych w małych ilościach. Niektóre środki dezynfekujące składają się z nadtlenku wodoru i katalazę stosuje się podzielić ten składnik przed ponownym użyciem soczewek.
działalność
Aktywność katalazy, enzymu zależy od wieku organizmu. Młodzi tkanki aktywności enzymu jest znacznie wyższa niż w starych. Wraz z wiekiem u ludzi i zwierząt aktywność katalazy stopniowo zmniejsza się w wyniku starzenia się tkanek i narządów.
Według ostatnich badań, spadek aktywności katalazy jest jedną z możliwych przyczyn siwienie włosów. Nadtlenek wodoru jest produkowany nieprzerwanie w organizmie człowieka, ale nie zaszkodzi – katalaza rozkłada się go szybko. Jednak, jeśli poziom tego enzymu jest ograniczona, to jest oczywiste, że nie cały nadtlenek wodoru jest katalizowana przez enzym. Tak więc barwę od wewnątrz włosy przez rozpuszczanie naturalnych barwników. To niespodziewane odkrycie obecnie testowane przez badaczy i może odgrywać rolę w rozwoju leków, zawieszania siwienie włosów.












