węglowodory aromatyczne mieć strukturę cykliczną. W pierwszym przedstawicielem tej serii – benzen (C 6H 6). Formuła odzwierciedla strukturę materii, pierwszy zaproponował chemika Kekule 1865. Według opowieści naukowca, miał długo rozważał tajemnicę benzenu. Pewnej nocy miał wąż gryzie własny ogon. Rankiem wzór strukturalny benzenu została już sporządzona. Było to pierścień 6 atomów węgla. Trzy z nich były w podwójnym wiązaniem.

Struktura benzenu
Węgla w węglowodorach aromatycznych stanowi sześciokąt foremny. Czasami podczas nagrywania reakcje równań przedstawiają jego wydłużony w kierunku pionowym. Ta grupa atomów ma specjalnej nazwy – pierścień benzenowy. Ustalenie struktury cyklicznej benzenu jest jego otrzymanie z trzech cząsteczek acetylenu – nienasyconego węglowodoru mającego potrójne wiązanie. Węglowodory aromatyczne są także nienasycone i wykazywać pewne właściwości charakterystyczne dla alkenów. Z tego powodu, w pierścieniu benzenowym przez trzy kreski, równoległych do powierzchni, należy zwrócić uwagę na obecność podwójnego wiązania. Taki wzór benzen nie w pełni odzwierciedlają stan atomów węgla w cząsteczce.
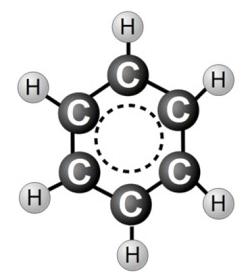
Benzen: Formuła, która odzwierciedla rzeczywistą strukturę
W rzeczywistości połączenie pomiędzy węgla w pierścieniu są sobie równoważne. Wśród nich nie było możliwe, aby przeznaczyć pojedyncze i podwójne. Taka cecha jest wyjaśnić strukturę elektronową benzenu, znamienny tym, że jądro węgla sp 2 w stanie -gibridizovannom podłączone do jego sąsiadów w pierścieniu, i trzy konwencjonalnych pojedynczych wiązań wodorowych. W tym przypadku sześciokąta, które znajdują się w tej samej płaszczyźnie 6 atomów węgla, a 6 – chlorowodoru. Tylko chmury elektronowej czwarty s elektronów nie biorą udziału w hybrydyzacji, rozmieszczone w różny sposób. Ich kształt przypomina hantle, ośrodek przypada na płaszczyzny pierścienia. Pogrubionej części znajdują się na górze i na dole. W tym przypadku, w pierścieniu benzenowym i poniżej są dwa gęstości elektronów napotykane s nakładające się chmurami elektronowymi. Istnieje ogólna wiązanie chemiczne z atomem węgla w pierścieniu.
Właściwości pierścienia benzenowego
Ze względu na całkowitą gęstość elektronów zmniejsza odległość pomiędzy atomami w pierścieniu. Są równe 0,14 nm. Jeśli w pierścieniu benzenowym istnieje pojedynczych i podwójnych wiązań, to dwa środki: 0,134 i 0,154 nM. Rzeczywistej struktury o wzorze benzenu nie zawierają wiązań pojedynczych i podwójnych. W związku z tym, węglowodory aromatyczne odnosi się do nienasyconych związków organicznych tylko formalnie. Składem przypominają alkenów, lecz mogą uczestniczyć w reakcji podstawienia, która jest charakterystyczna dla węglowodorów nasyconych. Aromatyczny pierścień benzenu posiada znaczną stabilność utleniaczy. Wszystkie te cechy pozwalają nam rozważyć pierścień specjalny rodzaj komunikacji – nie podwójne i pojedyncze.
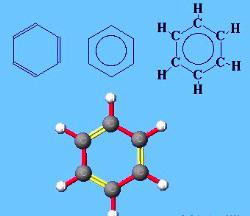
Jak przedstawiać wzór benzenu?
Prawidłowe formuła benzenowa trzech wiązań podwójnych, tak jak w Kekule, lecz w postaci sześciokąta z koła wewnątrz. Jest symbolem wspólnej tożsamości 6 elektronów.
Jest to potwierdzone przez strukturę symetrii właściwości substancji. pierścień benzenowy jest stabilna, ma znaczny sprzężenie energii. Właściwości pierwszym przedstawicielem węglowodorami aromatycznymi występuje w jego homologów. Każdy z nich może być przedstawione w postaci pochodnej, w którym podstawienie atomów wodoru z różnych rodników węglowodorowych.

















